Erä vahvoja kipulaastareita pois myynnistä tuotevirheen vuoksi
Lääketurvallisuus 02.09.2015 11:00 INKERI HALONEN KUVAN KÄSITTELY: E-R SEPPÄLÄ-HOLMBERG
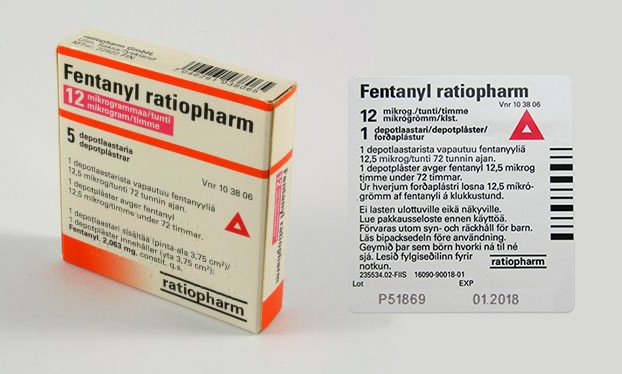
Kuvassa Fentanyl ratiopharm -kipulaastarin ulkopakkaus sekä poisvedettävän erän oikea laastarin suojapussi. Virheellisessä pussissa on vieraskielinen teksti.
Fentanyl ratiopharm -laastarierästä on löytynyt yksi virheellisen tuotteen sisältänyt pakkaus. Varotoimena koko erä poistetaan markkinoilta.
Ratiopharm Oy vetää pois myynnistä kivun hoitoon tarkoitetun Fentanyl Ratiopharm 12 mikrogrammaa/tunti -laastarierän P51869. Laastareissa on merkintä, että ne on käytettävä ennen 31.1.2018.
Suomessa on löytynyt yhdestä 12 mikrogramman lääkepakkauksesta vieraskielinen 25 mikrogramman laastari.
Tavallista vahvemman laastarin käyttö voi aiheuttaa käyttäjälleen hengenvaaran.
Pakkausvirheen mahdollisuutta ei voida sulkea pois muista pakkauksista, joten erä poistetaan varmuuden vuoksi markkinoilta.
Virheellistä erää on ollut apteekeissa myynnissä touko–elokuun ajan.
Virheellisen pakkauksen tunnistaa laastarin suojapussista
Ratiopharm Oy:n vastuunalainen johtaja Lasse Rautiainen tähdentää, että virheellisen pakkauksen tunnistaa laastarin suojapussin vieraskielisestä, eli hepreankielisestä tekstistä.
Oikeassa suojapussissa on suomenkielinen teksti ja Ratiopharmin tunnus.
Lääketukku Tamrosta on toimitettu nyt poisvedettävää erää apteekkeihin noin 1600 pakkausta.
Apteekin huumausainekirjapito helpottaa takaisinkeruuta
Kangasalan apteekissa vahvojen kipulaastareiden takaisinveto on sujunut hyvin, ja toistaiseksi vain yhdeltä asiakkaalta on löydetty kyseistä erää.
Pakkaus on parhaillaan matkalla apteekkiin, jossa mahdollinen tuotevirhe tarkistetaan.
– Huumausainekirjanpidosta näimme nopeasti, kenelle lääkettä oli toimitettu. Oli meidän onni, että kaikki toimitukset oli tehty hoitokoteihin, joten asiakkaat oli helppo tavoittaa, apteekin proviisori Laura Pantsar kertoo.
Mikäli kyseessä olisi ollut muun kuin huumausaineeksi luokiteltavan lääkevalmisteen poisvedosta, olisi sitä saaneiden asiakkaiden selvittäminen ollut huomattavasti työläämpää apteekille, Pantsar kuvailee.
Ratiopharm on yhdessä lääkealan turvallisuus- ja kehittämiskeskus Fimean kanssa ohjeistanut, että myös kuluttajien tulee palauttaa kyseisen erän pakkaukset apteekkiin.
Avaamattomat pakkaukset vaihdetaan korvaavaan valmisteeseen. Avattu pakkaus tarkistetaan apteekissa. Jos pakkaus on virheetön, se palautetaan takaisin asiakkaalle.
Fimean arvion mukaan poisveto ei aiheuta ongelmia lääkehoitojen jatkuvuuteen, koska korvaavaa erää on saatavilla.